La idea de que todas las sustancias en el mundo están compuestas de átomos nació en el siglo V a. C., cuando el antiguo pensador griego Demócrito sugirió que todo lo que existe está compuesto de las partículas móviles más pequeñas. Uno solo podría suponer que, muy probablemente, no carece de sentido. Durante muchos siglos después de Demócrito, los átomos fueron retirados periódicamente, pero esta hipótesis no era popular en aquellos tiempos remotos. En el siglo XIX, la hipótesis atómica reapareció en el horizonte científico.
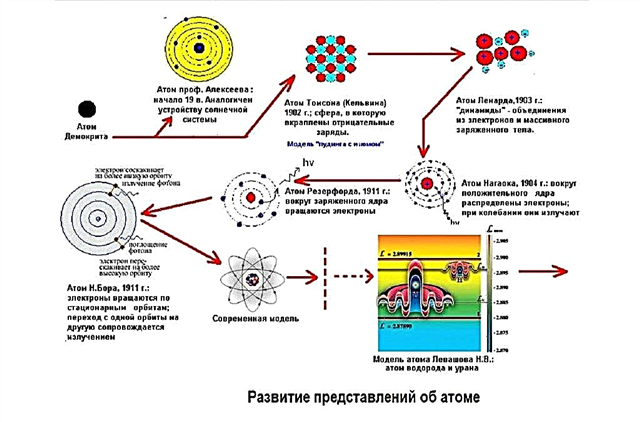
Modelos de estructura atómica

Los científicos estaban buscando un modelo que pudiera describir satisfactoriamente la imagen del mundo real. El átomo resultó ser un modelo muy adecuado. Aunque los átomos no se pueden ver, pero al permitirles existir, los científicos podrían explicar lo que observaron en sus experimentos y en la naturaleza.
Los científicos estaban convencidos de la existencia de átomos mucho antes de que pudieran probarlo. El modelo funcionó, aunque nadie pudo probar su verdad. Por ejemplo, a principios del siglo XIX, el científico inglés John Dalton, al estudiar las leyes de las reacciones químicas, descubrió que dos sustancias siempre reaccionan químicamente en la misma proporción constante. Por ejemplo, la combinación de una parte de oxígeno y dos partes de hidrógeno da agua.
Esto sugirió que los átomos de una sustancia, iguales en masa entre sí, se unieron con átomos de otra sustancia (es decir, con átomos de una masa diferente). En el caso de la formación de agua, un átomo de oxígeno se combina con dos átomos de hidrógeno.El modelo atómico ayudó a comprender lo que Dalton observó exactamente en sus experimentos. Hay más evidencia simple de la existencia de átomos.
Si observa con un microscopio las partículas de polen suspendidas en el agua, puede ver que hacen movimientos caóticos. ¿Por qué? Los científicos han sugerido que esto puede deberse al hecho de que las partículas de polen colisionan con numerosos átomos o grupos de átomos que los científicos han llamado moléculas (por ejemplo, las partículas en el agua chocan con las moléculas de agua).
¿En qué consiste un átomo?
Los científicos que estaban de acuerdo con la teoría atómica creían que un átomo consiste en pequeñas partículas cargadas eléctricamente, positivas y negativas, que, cuando se combinan en un átomo, como en una bola, se neutralizan entre sí y hacen que el átomo como un todo sea eléctricamente neutro. Pero en 1907, el físico inglés Ernest Rutherford, con sus experimentos, demostró que esto no es del todo cierto.
Experiencia Rutherford
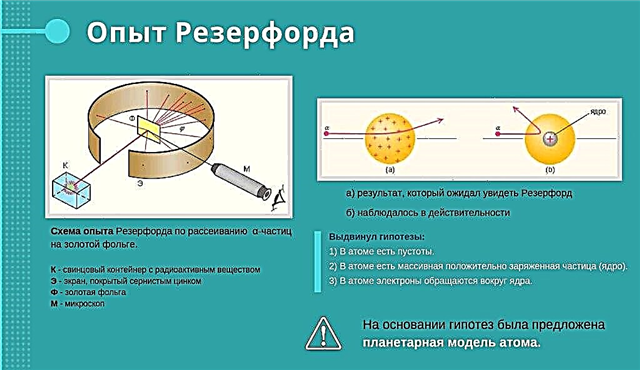
Rutherford bombardeó una lámina de oro con un haz de alta velocidad de partículas cargadas positivamente. Él creía que las partículas pasarían a través de la lámina. Algunas partículas cargadas positivamente volaron a través de la lámina. Y algunos no pudieron hacer esto. Además, rebotaron en el experimentador, como si alguna fuerza oculta en la lámina los alejara. Rutherford estaba sorprendido. Dijo que era lo mismo que comenzar a quemar la olla en papel fibroso y de repente ver cómo la olla sale volando de la frente del alfarero.
Modelo de átomo planetario - Atom Core
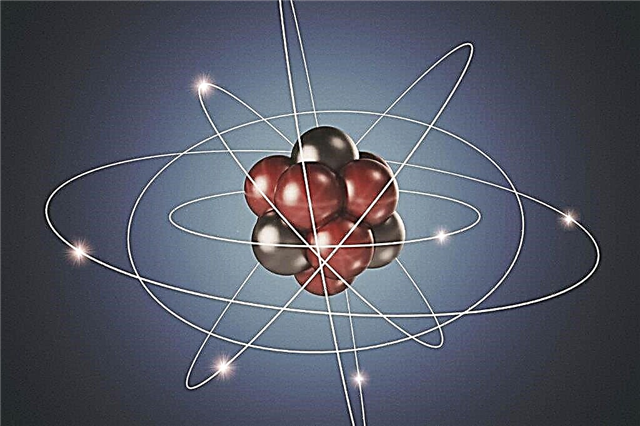
Los experimentos de Rutherford ayudaron a confirmar la hipótesis atómica y comprender cómo funciona el átomo. Quedó claro que las partículas positivas y negativas no están distribuidas uniformemente en el átomo. Si esto fuera así, entonces las partículas cargadas positivamente en el experimento de Rutherford no serían repelidas con tanta fuerza. Por lo tanto, el núcleo de un átomo no es neutral. En el medio del átomo hay una bola densa de partículas, es decir, en el medio, que se llama núcleo del átomo, hay protones cargados positivamente y neutrones neutros.
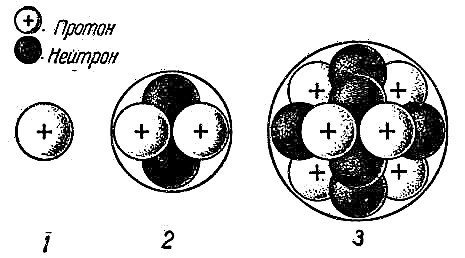
A una distancia considerable del núcleo, las partículas cargadas negativamente (electrones) giran alrededor de sus órbitas a su alrededor. Como una carga positiva es igual en valor a una carga negativa, el átomo en su conjunto es eléctricamente neutro. No tiene ningún cargo.
Pero el núcleo mismo es la concentración de una carga positiva. Muchas de las partículas positivas en el experimento de Rutherford volaron demasiado cerca del núcleo cargado positivamente de un átomo de oro. Como las cargas positivas se repelen mutuamente, estas partículas volaron hacia el experimentador. Esto le llevó a la idea de cómo están realmente dispuestos los átomos.
Quarks
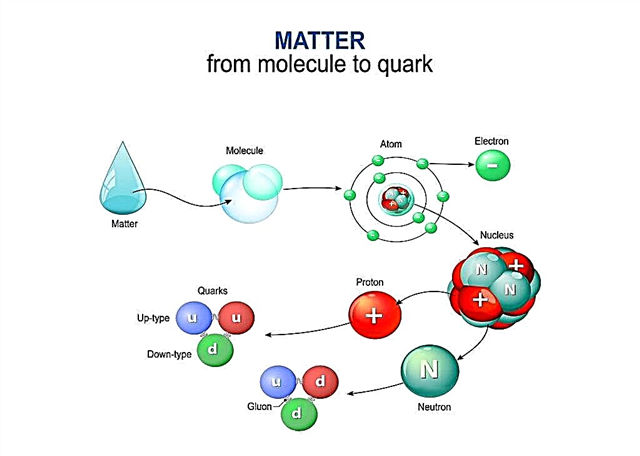
Los protones y los neutrones son partículas que, aunque pequeñas, están formadas por partículas aún más pequeñas llamadas quarks. Hoy, los científicos creen que los protones y los neutrones están formados por partículas aún más pequeñas llamadas quarks.
Quarks es un nuevo modelo que explica mejor el comportamiento de los átomos en el mundo real. Y así como los científicos habían buscado previamente evidencia experimental de la existencia de átomos, ahora están buscando evidencia real de quarks.